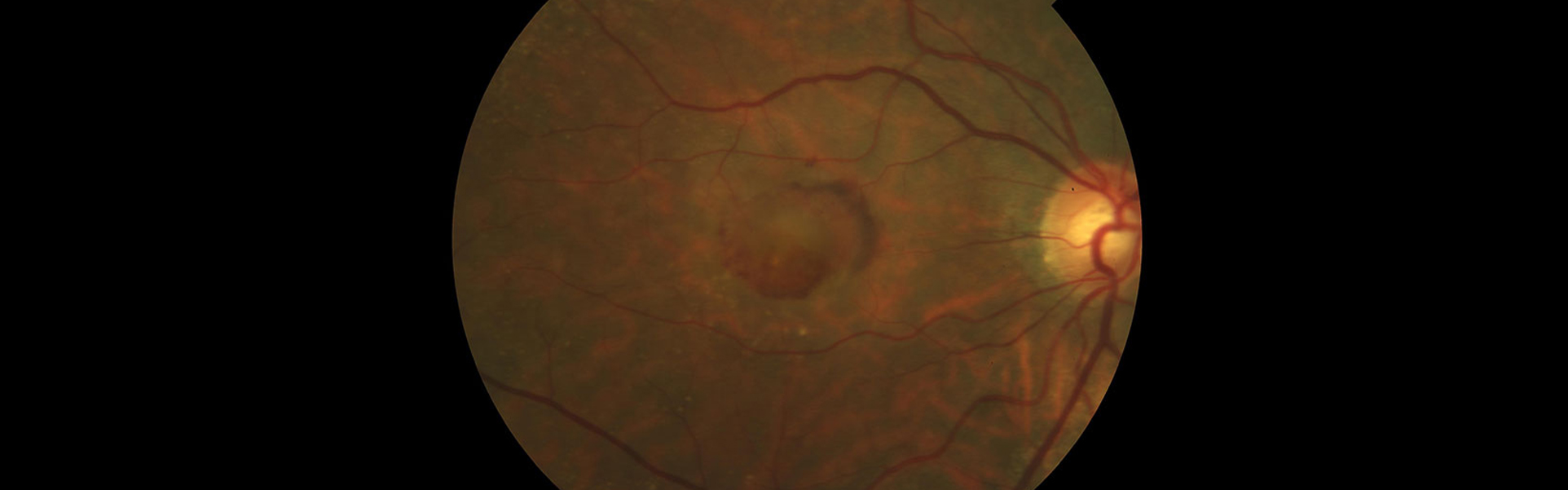
Maculopatia
La degenerazione maculare legata all’età (DMLE) rappresenta la prima causa di ipovisione nei soggetti con età superiore ai 50 anni nei paesi industrializzati.
La DMLE è una patologia di origine multifattoriale che coinvolge la regione centrale della retina, denominata macula. Si tratta, volendo semplificare, di un invecchiamento troppo rapido della macula. Questa malattia, sebbene possa causare importanti danni alla visione centrale, non è causa di cecità totale perché la macula rappresenta solo una piccola porzione della retina che, se intatta, permette una preservazione del campo visivo periferico.
La conoscenza e la presa in carico della DMLE sono in continua evoluzione grazie ai recenti progressi in ambito genetico, terapeutico e diagnostico.
La retina è un tessuto nervoso che tappezza il fondo dell’occhio ed è responsabile della trasformazione del segnale luminoso in elettrico, che viene in seguito trasmesso al cervello attraverso il nervo ottico.
La macula è una regione particolare della retina, che permette una visione ad alta definizione di ciò che si intende osservare (testi, dettagli in un quadro, visi di persone,…), grazie all’alta concentrazione di cellule della visione (fotorecettori, in particolare i coni) presente al suo interno.
Considerando tutti i tipi di DMLE, senza distinzioni per forma o gravità, la prevalenza è di circa il 10% nella popolazione italiana.
Tuttavia, una divisione secondo l’età permette di evidenziarne un rapporto lineare con la prevalenza della patologia
1% nella popolazione tra 50 e 55 anni
10-12% tra 55 e 65 anni
15-20% tra 65 e 75 anni
25-30% oltre i 75 anni
La presenza di una predisposizione genetica per la DMLE è testimoniata dall’osservazione di famiglie con più alta prevalenza di patologia così come da gemelli che presentano quadri clinici simili. Effettivamente, il rischio di DMLE è circa 4 volte più alto se in famiglia è presente un parente affetto.
Sono stati testati numerosi geni ritenuti potenzialmente coinvolti nella genesi della patologia, tra cui i più importanti codificano per proteine coinvolte nell’infiammazione (fattori del complemento B,C,H).
La maggior incidenza di DMLE in alcune popolazioni ha permesso di identificare un ruolo importante giocato dall’ambiente e dallo stile di vita. Il fumo di tabacco aumenta da 3 a 6 volte il rischio di DMLE mentre la una supplementazione vitaminica (C ed E) e di alcuni minerali ha permesso di dimostrare, con lo studio AREDS, una riduzione del rischio di progressione della patologia di circa il 25%.
Stadiazione della patologia
Questi segni si osservano nel 30% della popolazione oltre i 75 anni e solo una minor parte dei soggetti affetti da DMLE negli stadi precoci evolverà verso stadi più avanzati.
La patologia si manifesta con piccoli depositi, chiamati drusen, di materiale di scarto proveniente dai fotorecettori. Sebbene questo materiale di scarto sia prodotto durante tutto il corso della vita, nei pazienti maculopatici il suo smaltimento è rallentato o non funzionante.
Oltre alla presenza di drusen si osservano anche alterazioni a carico dell’epitelio pigmentato retinico, uno strato cellulare posto esternamente al tessuto neuroretinico.
In questa fase di patologia il paziente è spesso asintomatico e la diagnosi è a cura dell’oculista attraverso l’esame del fondo oculare e, più precisamente, l’OCT.
Un progressivo e più o meno rapido aggravamento delle forme precoci, passando per forme dette intermedie, può portare allo sviluppo di complicanze, uni o bilaterali, che caratterizzano gli stadi avanzati della patologia, divisi in forme atrofiche e forme neovascolari.
DMLE neovascolare (o “umida”)
Sebbene meno frequente rispetto alla forma atrofica, è responsabile del 90% delle cecità legali tra i pazienti affetti da DMLE. Questa forma è caratterizzata dalla formazione di capillari anomali (neovasi) entro/sotto la retina o sotto l’epitelio pigmentato retinico. La genesi dei neovasi capillari non è del tutto nota ma alla base vi sono stimoli ipossici ed infiammatori legati a condizioni di fragilità locale. I neovasi hanno una struttura più fragile rispetto ai capillari normali e la loro parete permette il passaggio di siero o sangue che si accumulano sotto o entro il tessuto retinico. L’accumulo di liquido intra o sottoretinico è responsabile di una tossicità cellulare diretta così come della comparsa di sintomi quali abbassamento della visione, visione deformata (metamorfopsie), alterazioni della percezione dei colori o del contrasto.
L’evoluzione spontanea di queste lesioni è generalmente verso la formazione di cicatrici, che hanno un’evoluzione più lenta ma che lasciano gravi alterazioni a carico della visione centrale.
Per le forme di DMLE neovascolari esistono ad oggi dei trattamenti farmacologici, principalmente atti a limitare il danno provocato dai neovasi capillari. Essendo l’efficacia di questi trattamenti anche funzione dello stadio evolutivo del quadro clinico la tempestività del controllo specialistico, della diagnosi e del successivo trattamento sono essenziali.
Il rischio che la DMLE coinvolga entrambi gli occhi è del 10% a 1 anno e del 42% a 5 anni.
DMLE atrofica (o “secca”)
La DMLE atrofica è la forma avanzata più frequente, contando oltre il 75% dei casi. Essa è dovuta a una progressiva degenerazione delle cellule retiniche, a partenza centrale o paracentrale con possibile progressiva estensione alle zone circostanti.
I primi segni percepiti dal paziente sono in genere la difficoltà nella lettura, nella scrittura o nel riconoscimento dei visi delle persone.
La DMLE atrofica ha un’evoluzione lenta e generalmente permette ai pazienti un relativo adattamento, utilizzando per la fissazione le aree maculari preservate.
Sebbene molti sforzi e numerosi trial clinici siano stati condotti al fine di rallentare l’evoluzione della DMLE atrofica, non esiste ad oggi un trattamento in grado di ripristinare i tessuti danneggiati o di rallentarne significativamente la progressione.
Sintomi della DMLE
Possono essere variabili, in funzione dello stadio di patologia, dell’evolutività e della sensibilità del paziente.
Negli stadi più precoci, la DMLE può provocare lievi deficit visivi o minime alterazioni della percezione dei colori spesso non riportati dal paziente ma osservabili con l’esame del fondo dell’occhio o con l’OCT.
Con la progressione del quadro clinico, la visione centrale può scendere più o meno rapidamente ed il paziente può accorgersi di avere maggior difficoltà nella lettura o nella scrittura così come nel riconoscimento di visi di persone in televisione.
La comparsa di piccole aree di alterazione della visione, percepite come “macchie nere” (scotomi) è tipica della DMLE secca o della forma umida in stadio cicatriziale.
La visione deformata è tipica di entrambe le forme ma la sua repentina comparsa è indice di alterazioni intraretiniche prodotte da neovasi capillari (forma umida).
Siccome l’insorgenza della DMLE è più spesso asimmetrica (inizia da un occhio per poi eventualmente coinvolgerli entrambi), può essere difficile riconoscere i primi sintomi di patologia tenendo entrambi gli occhi aperti: è pertanto necessario chiudere prima un occhio e poi l’altro per valutare la funzione del singolo.
L’auto-monitoraggio dei sintomi è essenziale e può essere fatto al domicilio: chiusura alternata degli occhi per valutare la capacità del singolo occhio di valutare immagini di riferimento (ad esempio i dettagli di un albero fuori dalla propria finestra) e per valutare con buona approssimazione la comparsa o la progressione delle metamorfopsie utilizzando una specifica griglia (stampata o su tablet), chiamata test di Amsler.
In caso di comparsa o aggravamento dei sintomi descritti, è raccomandato un controllo specialistico tempestivo.
E’ sempre bene ricordare che la macula, occupando solo il 2-3% della superficie retinica, è responsabile della visione centrale e pertanto un suo deterioramento anche grave non compromette la visione periferica.
Diagnosi di DMLE
Fondo oculare e retinografia
Una visita oculistica completa con valutazione del fondo oculare può mettere in luce stadi più o meno avanzati di DMLE: presenza di drusen, alterazioni a carico dell’epitelio pigmentato retinico, presenza di edema maculare, presenza di emorragie.
La retinografia a colori (foto del fondo oculare) permette di creare un “fermo-immagine” della situazione del paziente utile per futuri confronti e permette inoltre di mostrare al paziente le lesioni in questione. L’utilizzo di specifici filtri (luce infrarossa, aneritra, ecc) permette di distinguere con maggior facilità alterazioni specifiche (ad esempio emorragie o aneurismi con luce aneritra).
Tomografia a coerenza ottica
L’OCT è ormai considerato il gold standard nella diagnostica della DMLE, in qualunque stadio.
Rispetto alle tecniche precedentemente utilizzate, l’OCT è ora maggiormente diffuso in quanto di facile realizzazione, di relativamente facile interpretazione e non invasivo.
L’OCT permette un’analisi frontale e trasversale della retina, dell’epitelio pigmentato e della coroide sottostante, con una risoluzione d’immagine pari a pochi micron.
Le drusen, le alterazioni dell’epitelio pigmentato, le cisti intraretiniche, il fluido sottoretinico, i distacchi dell’epitelio pigmentato retinico possono essere diagnosticati con assoluta certezza ed è possibile seguirne l’evoluzione nel tempo grazie a modalità di follow up.
OCT angiografia
Questa metodica, di più recente introduzione, è in grado di valutare i cambiamenti (o decorrelazioni) all’interno di un tessuto esaminato.in due momenti a distanza di tempo nota. In sostanza, l’OCT-A permette la visualizzazione del flusso ematico all’interno del tessuto retinico: arteriole, venule, capillari, neovasi.
E’ una metodica in grado di diagnosticare con sicurezza medio-alta (variabile a seconda delle caratteristiche della DMLE neovascolare) la presenza di neovasi all’interno o al di sotto del tessuto retinico.
Si tratta di tecniche di imaging tradizionale il cui utilizzo è sempre più raro grazie alla possibilità di diagnosi sempre più precise utilizzando esami non invasivi (OCT e OCT-A). Queste metodiche permettono la visualizzazione della vascolarizzazione retinica e coroideale a seguito della stimolazione con luce a lunghezza d’onda definita di particolari mezzi di contrasto (fluoresceina e verde di indicianina) iniettati per via endovenosa al momento dell’esame.
La necessità di utilizzare un mezzo di contrasto rende queste tecniche non prive di rischi di tipo allergico o di intossicazione in caso di alterata funzione epatica o renale. Tuttavia l’angiografia, considerata il gold-standard nella diagnosi e follow-up della DMLE essudativa, ha la peculiarità di essere un esame dinamico, che permette una diretta visualizzazione del flusso ematico e quindi di eventuali neovascolarizzazioni e può essere un esame necessario anche ai giorni nostri.
Autofluorescenza: permette di valutare, in modo non invasivo (senza mezzo di contrasto) la condizione del pigmento retinico. E’ utile per la diagnosi di patologie specifiche (e.g. degenerazione maculare pseudovitelliforme) e per il follow-up delle DMLE atrofiche.
Perimetria statica e dinamica: permette di definire la presenza e quantificare le dimensioni dello scotoma determinato dalla patologia e la preservazione del campo visivo periferico (principalmente utilizzato per fini medico-legali).
Microperimetria: permette la definizione della sensibilità luminosa retinica punto per punto grazie alla sovrapposizione di un’immagine retinografica (foto del fondo oculare). Può trovare un utilizzo soprattutto nella riabilitazione del paziente con scotoma centrale, per aiutarlo nel trovare un punto di fissazione alternativo.
Trattamento della DMLE
Nella DMLE iniziale, caratterizzata da drusen e alterazioni dell’epitelio pigmentato retinico, si sensibilizza il paziente a ridurre eventuali fattori di rischio, si incentivano una dieta ricca in pesce grasso e verdure a foglia verde, un’attività sportiva moderata e regolare e si propongono integratori alimentari specificamente studiati per la DMLE. Gli integratori alimentari nella DMLE vengono prodotti sulla base di quanto osservato negli studi AREDS (age-related diseases study) e AREDS 2 e contengono: vitamina C, vitamina E, zinco, rame, luteina e zeaxantina.
Gli integratori in commercio sono tantissimi e le differenze tra loro sono soprattutto in termini di addizione di altre sostanze (ad es vitamina D, acido alfalipoico, …). L’assunzione di questi integratori non ha l’obiettivo di far regredire la patologia quanto piuttosto quello di rallentarne l’evoluzione nel tempo. E’ stata dimostrata nell’AREDS 2 una riduzione di progressione verso forme più avanzate di DMLE nell’ordine del 20% a 5 anni.
Sono stati effettuati numerosi tentativi, negli anni passati, di trattamento della DMLE atrofica con lo scopo di arrestarne o rallentarne la progressione (e.g. inibitori del complemento, brimonidina) senza però arrivare ai risultati sperati.
E’ molto importante in questo stadio di patologia, effettuare visite di controllo regolari con esame del fundus e OCT per valutare la progressione di patologia
Nella DMLE avanzata, nella forma essudativa, il trattamento ha lo scopo di rallentare o bloccare l’attività neovascolare.
Dopo anni in cui il trattamento laser è stato considerato la prima linea, questo posto è ora ricoperto dagli anti-VEGF (vascular endothelial growth factor).
Attualmente sono disponibili due molecole on-label (ranibizumab: Lucentis e aflibercept: Eylea) ed una off-label (bevacizumab: Avastin) per il trattamento della DMLE neovascolare.
Le molecole differiscono per struttura, peso e target di azione.
Le differenze tra le molecole a disposizione si traducono in regimi di trattamento differenti, ma ad oggi una significativa superiorità di un farmaco rispetto all’altro nel trattamento della DMLE neovascolare non è stata dimostrata.
La DMLE essudativa di prima diagnosi (cosiddetta naive) viene generalmente trattata con iniezioni intravitreali mensili per i primi tre mesi. Al termine dei tre mesi viene normalmente effettuato un bilancio in cui si valutano la risposta funzionale (l’acuità visiva) e soprattutto la risposta anatomica (stato di attività della neovascolarizzazione all’OCT). Sulla base di questa valutazione si sceglie il tipo di regime di trattamento da proporre al paziente.
I principali regimi di trattamento sono: fisso, prorenata e treat and extend.
Il regime di trattamento ed il farmaco impiegati
Il regime fisso prevede iniezioni intravitreali a distanza temporale fissa tra loro (mensili o, in caso di aflibercept, bimestrali).
Il regime PRORENATA prevede iniezioni intravitreali a distanza variabile nel tempo, quando ritenuto necessario per riattivazione della patologia. Il regime prorenata prevede pertanto che il paziente venga valutato ogni mese al fine di osservare stabilità o progressione del quadro clinico.
Il regime TREAT AND EXTEND, di più recente introduzione, prevede iniezioni e visite di controllo a distanza variabile nel tempo, stabilita all’ultimo controllo. Lo scopo di questo trattamento è quello di ridurre il numero di iniezioni in quei pazienti con patologia meno attiva, andando ad individuare nel modo più preciso possibile l’intervallo temporale di recidiva della patologia. Ad esempio, in caso di stabilità a 3 mesi, il paziente sarà iniettato e rivalutato a 3,5 mesi mentre in caso di recidiva sarà iniettato e rivalutato a 2,5 mesi.
Nella maggioranza dei casi, il numero di iniezioni all’anno si riduce con il tempo dalla diagnosi, con una media di 5 iniezioni per anno nel secondo anno.
Dopo alcuni mesi dall’inizio del trattamento è possibile anche valutare l’efficacia del farmaco somministrato ed, eventualmente, sostituirlo con altre molecole qualora la risposta non sia soddisfacente.

